发布时间:2018-06-05 09:36 类别:医学前沿资讯 标签: 来源:转化医学网 作者:医学资源分享
近日,权威期刊《Science》杂志发表一篇顶级医学机构约翰霍普金斯大学的重磅研究,他们开发出一次检测8种癌症的方法。

肿瘤无疑是最让人害怕的疾病,人人避之犹恐不及!
然而,肿瘤却不是一个看得见的“敌人”,它在暗处,你想躲它真是非常不容易,平常你看不见也摸不着,等到感觉身体某个地方不舒服,去医院拿X光(或者其他手段)一查看,终于看到它在某个组织器官如同一个“小恶魔”一般趴在那里吸血。
“多想能够早点发现啊”,有无数患者曾经这么说过。

▲研究者们在《科学》杂志上面发表的文章
然而,要早点发现肿瘤谈何容易!实际上,很多成人的肿瘤从初期病变发展到晚期要经历长达20-30年的时间。如何在早期检测到肿瘤,特别是在影像学能检测到肿瘤之前发现病变,是医学界的一个重要的研究方向。
近日,约翰·霍普金斯大学的研究团队最近研发了一种早期肿瘤筛查方法,可以同时检测出8种常见肿瘤。这种名为CancerSEEK的液体活检技术,对8种常见肿瘤检测的中位敏感性达到了70%,特异度高达99%。对卵巢癌和肝癌的敏感性最高,随后则是胃癌、胰腺癌、食道癌和结直肠癌,检出敏感性均达到了60%以上【1,2,3】。
▶液体活检◀
液体活检,是Liquid Biopsy翻译过来的,顾名思义,就是把液体拿来做检测。
这中间就涉及到两个问题,第一,检测什么呢?第二,拿什么液体来检测呢?
尽管液体活检针对的疾病范围也较为广泛,然而,大多数时候还是针对肿瘤尤其是实体肿瘤而言的。

由于肿瘤在发生发展的过程中,一些肿瘤相关的物质比如肿瘤细胞、外泌体、肿瘤细胞裂解之后的DNA片段、肿瘤的代谢产物等等会进入血液或者其他组织液体中,因此,只要发明一些方法来检测这些物质是否存在或者含量是否比正常健康人高,就可以反映出这个人是否可能得了肿瘤。
那么,液体活检检测什么呢?
主要可以泛指检测血液或者其他液体中的比如循环肿瘤细胞(CTCs)、ctDNA、外泌体(exosome)等等在肿瘤患者中特异或者含量比正常健康人高的物质。
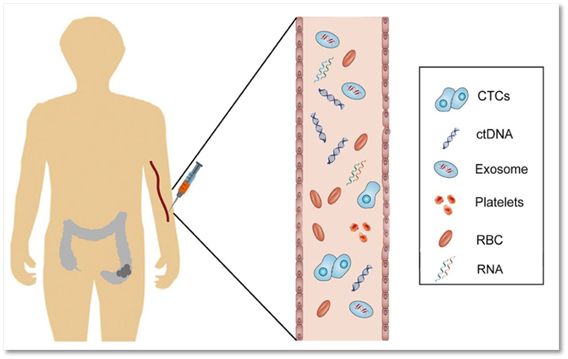
▲液体活检检测的常见物质,包括循环肿瘤细胞CTCs、ctDNA以及外泌体等等[4]
那么,液体活检检测哪些液体呢?
这个好说,只要是身体中的液体都可以好好地探究一番,比如最常见的是血液。其他常见的还有尿液(Urine)、唾液(Saliva),另外还有脑脊液(Cerebrospinal fluid)以及精液(Seminal plasma)等。
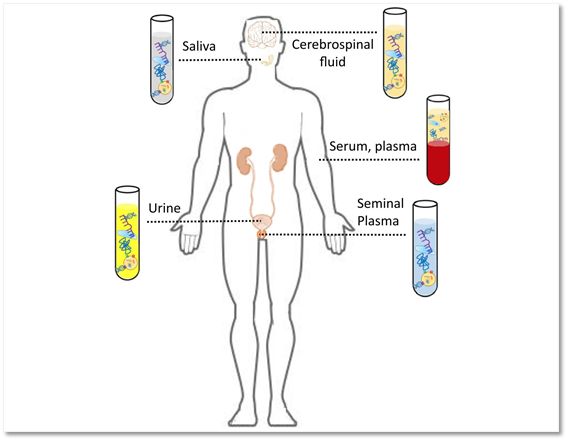
▲液体活检检测的常见液体[5]
总而言之,只要是液体就行,但是液体活检的原则是非侵入,通俗地讲就是取液体的时候不要损伤组织器官,比如你为了获得内某些液体,开肠破肚这样的大动干戈那就失去了液体活检的意义了,最好就是搜集唾液、尿液、血液等就能够判断或者辅助诊疗就行。
然而,液体活检目前也面临一定的挑战:
1. 对于早期肿瘤检测灵敏度还不够。早期肿瘤每毫升血清含有的致病突变常少于1个拷贝,这低于目前液体活检检测范围的下限;
2. 液体活检迄今为止还没有大规模的健康对照人群实验,而这对特异性的评估很关键;
3. 液体活检无法分辨出致病突变的来源。在影像学不能检出的早期阶段,确定肿瘤来源是非常重要的。
▶CancerSEEK◀
这篇研究的研究者们把他们发明的这种检测肿瘤的技术叫做CancerSEEK,那么,它有什么独特的呢?或者说比现有的检测肿瘤的液体活检技术有什么领先的地方呢?
实际上,这篇研究中采用的液体活检方法最大的特色之一恐怕在于结合了ctDNA检测和血液中肿瘤蛋白标志物共同来做判断(如下图所示)。

▲这篇《科学》论文采用的CancerSEEK技术的示意图,抽取血液,测定里面的ctDNA及肿瘤相关的标志蛋白,从而联合这两方面的数据来判断肿瘤(图片来自约翰霍普金斯大学网站)
这就像1加1大于2,联合两个方面的证据来检测癌症,准确性自然会更高一些。简单通俗地说来,研究者们就是首先利用ctDNA的突变来判断一个人是不是得了肿瘤,接着,再利用常见的八种血液中的蛋白标志物来判断到底得的是哪一种肿瘤。
举个例子,研究者们首先测定一个人血液中的ctDNA有p53突变、PTEN突变、EGFR突变、BRAF突变等(研究者一共检测了16个基因中的61种突变),就可以判断这个人得了肿瘤了,但这个时候还并不知道她得的是什么肿瘤。因此,接着就需要使用各种肿瘤的较为特异的血液标志物来判断了,比如,此时检测到血液标志物CA125蛋白,那么结合ctDNA的数据就知道这个人得了卵巢癌,因为CA125是卵巢癌中较为特异地高表达。
▶16种基因的61个突变◀
那么,研究者们怎么来检测ctDNA的呢?或者比以往的检测ctDNA的技术有什么改进之处呢?
并且,最关键的是,为何要选16中肿瘤相关基因的61个突变呢?而且又是哪16个基因呢?
这里,小编先要科普一下什么是ctDNA?必须要注意ctDNA和cfDNA的区别。
循环肿瘤DNA(circulatingtumor DNA,ctDNA),是一种存在于血浆或血清、脑脊液等体液中的细胞外DNA,主要来自于坏死或凋亡的肿瘤细胞、肿瘤细胞分泌的外排体及循环肿瘤细胞,大小通常为160-180bp。ctDNA是游离DNA(cell-free DNA,cfDNA)中的一类,所占比例较低(0.1%-1%之间),因而检测难度较大。
因此,ctDNA检测难度大,故而这篇文章的研究者们就在这个ctDNA检测上面下功夫。
采用ctDNA如何判断的了肿瘤呢?
这篇研究者们的科研思路其实与其他这个领域的研究者没什么不同,就是普通的思路,既然ctDNA是肿瘤细胞死亡或者凋亡而来,那么,肿瘤细胞中的常见突变基因比如P53、PTEN、KRAS、BRAF、EGFR、APC、PIK3CA等的突变小片段也包含在这些ctDNA之中,这样一来,只需要检测ctDNA的上述基因的突变,便可以判断是否身体中具有肿瘤细胞了(尽管此时还不知道是哪一种肿瘤,因为大多数肿瘤都有相同的基因突变,比如大多数都包含P53基因突变)。

▲检测ctDNA的61个基因突变位点之后进入敏感性的平台期,继续增加突变位点的检测对判断肿瘤帮助没有显著提高;图中纵坐标表示肿瘤的检出比例,横坐标表示ctDNA突变位点的检测数量
研究者们筛选了16个常见的在肿瘤中常见的广泛突变的基因,除了上述的P53、PTEN、KRAS、BRAF、EGFR、APC、PIK3CA之外,还包括NRAS、FGFR2、AKT1、PPP2R1A、GNAS、HRAS、CDKN2A、FBXW7。
有了这16个基因之后,研究者们再针对每个基因设计的多个突变位点进行扩增,比如针对PETN这个基因,研究者们就设计了4个位点的突变扩增;又比如APC这个基因,设计了2个扩增位点;而P53扩增的突变位点最多。因此,针对这16个基因,研究者们设计了61个突变位点扩增用于检测。
▶8种肿瘤血液标志物◀
前面检测ctDNA主要是判断得没得癌症,然而,并不知道得了哪种癌症。
因此,研究者们就必须要结合各种癌症的血液中的标志物蛋白来判断到底是哪种肿瘤。
所以,为了检测8种常见的肿瘤,研究人员从41种这些肿瘤的产物中精选出8种对于鉴别健康人和肿瘤患者特别有效的蛋白质,哪八种呢?
包括:CA-125、CEA、CA19-9、Prolactin、HGF、OPN、Myeloperoxidase、TIMP-1这八种。
▶联合的力量◀
那么,结果如何呢?效果是否让人满意呢?
应该说效果还是比较理想的,CancerSEEK技术对于肿瘤检测的中位敏感性达到了70%。
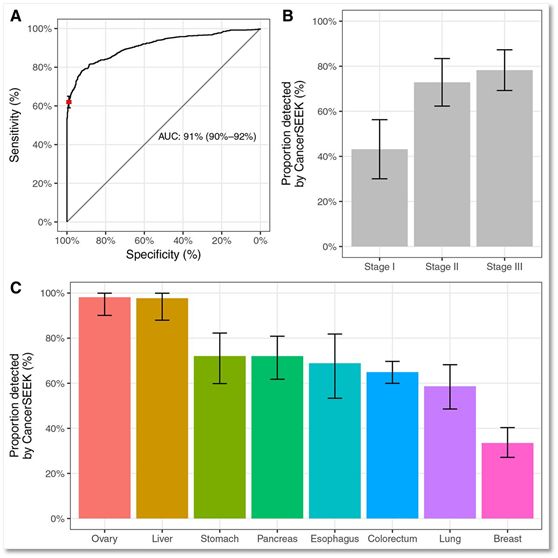
▲CancerSEEK检肿瘤的效果;(A)ROC曲线;(B)对各个时期的肿瘤检测的比例,可以看出,对于I期肿瘤检测的效果稍差;(C)对各种肿瘤检测的效果
其中CancerSEEK这一方法对于卵巢癌和肝癌的敏感性最高,随后则是胃癌、胰腺癌、食道癌和结直肠癌,均达到了60%以上。
对于肺癌(<60%)和乳腺癌(33%)的敏感性虽然稍差,但好在这些肿瘤还是能够通过胸部LDCT或乳腺摄片等其他手段来早期检测。
▶别欢喜太早◀
宣传科学知识一定要看看不足之处,否则很容易让大众以为这个问题已经被科学家解决了,比如,常常见到新闻报道说这种病被攻克了,那种病被治愈了,还有什么攻克癌症等等,不一而足。
这个号称能够一次检测8种癌症的方法实则也有一定的缺陷,可能导致其并不如报道的那样神奇。
最关键的问题是什么,且不说ctDNA突变检测的各种问题,单就这个“肿瘤血液标志物蛋白”到底能不能判断某种肿瘤至今在都还有争议。比如最常见的,癌胚抗原CEA,可能与消化道的恶性肿瘤相关,但也可能与吸烟、怀孕、肠炎、糖尿病、心血管疾病等相关,因此,即便检测到CEA也不能肯定就是得了某种癌症了。

并且,这里还要提醒注意一下,不要以为这种方法就像测个血糖一样,针扎一下就能测了,以前人们也被“滴血测癌”多次忽悠过。小编看了看原文的实验方法,貌似测定上面的ctDNA都需要7.5毫升血清,粗略地算一下这意味着15毫升血液,这说明这种方法一次也得抽一小管血液,并不会像测个血糖一样方便的。

参考资料:
1.Detection and localization of surgicallyresectable cancers with a multianalyte blood test.
2.https://www.hopkinsmedicine.org/news/media/releases/single_blood_test_screens_for_eight_cancer_types
3.‘Liquid biopsy’for cancer promises early detection.
4. Shiyu Jia, Rui Zhang, Ziyang Li, &Jinming Li. (2017). Clinical andbiological signi cance of circulating tumorcells, circulating tumor DNA, andexosomes as biomarkers in colorectal cancer.Oncotarget, 2017, Vol. 8, (No. 33), pp: 55632-55645.doi:10.18632/oncotarget.17184.
5. Meo, A. D., Bartlett, J., Cheng, Y.,Pasic, M. D.,& Yousef, G. M. (2017). Liquid biopsy: a step forward towardsprecisionmedicine in urologic malignancies. MolecularCancer,16(1), 80.doi: 10.1186/s12943-017-0644-5.